Dlaczego diament jest najtwardszym materiałem? – MÓZGOTRON
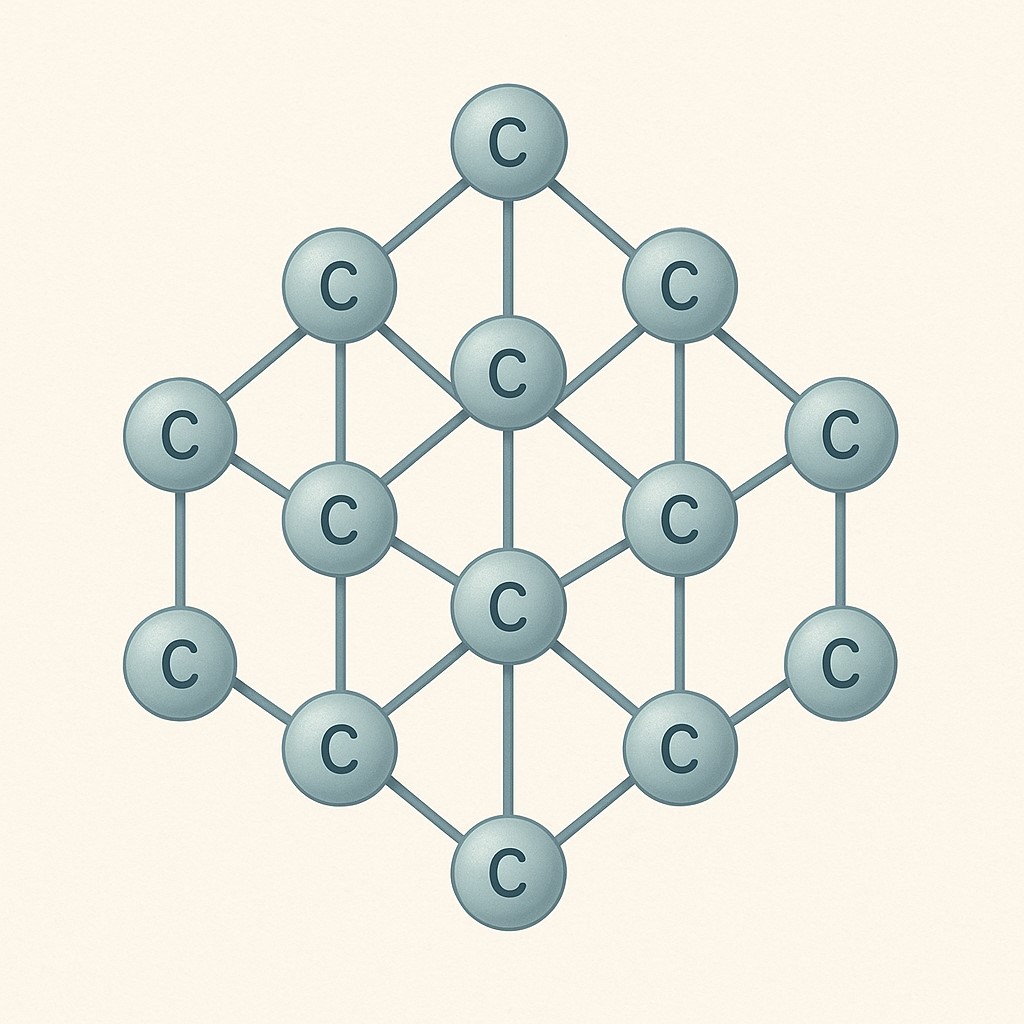
Diament jest odmianą węgla (C), w której atomy są połączone kowalencyjnymi wiązaniami o bardzo dużej energii. Każdy atom węgla w diamencie ma hybrydyzację sp³ i tworzy cztery bardzo silne wiązania z czterema sąsiednimi atomami.
1. Trójwymiarowa sieć wiązań sp³
Struktura kryształu diamentu to trwała, regularna sieć przestrzenna, w której:
C−C−C
tworzy sztywną, powtarzalną kratownicę. Nie ma w niej „płaszczyzn poślizgu”, które mogłyby pozwolić atomom przemieścić się względem siebie — jak w metalach.
2. Silne wiązania kowalencyjne
Energia jednego wiązania C–C w diamencie wynosi około:
∼350 kJ/mol
co jest jedną z najwyższych wartości dla wiązań pojedynczych w związkach chemicznych.
A ponieważ cały kryształ to ciągła sieć takich wiązań, do mechanicznego zniszczenia trzeba naraz przerwać ogromną liczbę bardzo silnych połączeń.
3. Brak defektów i porządna struktura
Diament ma wysoki stopień uporządkowania, co oznacza, że nie posiada wielu defektów kryształów osłabiających strukturę (jak to ma miejsce np. w grafitach, metalach czy polimerach). Mniej defektów → mniej punktów, od których mogłoby zacząć się pękanie.
Twardość diamentu wynika z trójwymiarowej sieci silnych wiązań kowalencyjnych C–C (sp³), które nie pozwalają atomom przesunąć się względem siebie, co czyni go niezwykle odpornym na zarysowanie i odkształcenie.

